Sebentar
lagi kita akan kedatangan tamu istimewa, Hari Raya ‘Idul Adha, dimana di hari
itu dan hari tasyrik dilakukan penyembelihan hewan qurba. Jika Anda belum
memutuskan untuk berkurban tahun ini, ada baiknya Anda menyimak hikmah dan
keutamaan qurban pada hari-hari tersebut:
1. Kebaikan
dari setiap helai bulu hewan kurban
Dari Zaid
ibn Arqam, ia berkata atau mereka berkata: “Wahai Rasulullah SAW, apakah qurban
itu?” Rasulullah menjawab: “Qurban adalah sunnahnya bapak kalian, Nabi
Ibrahim.” Mereka menjawab: “Apa keutamaan yang kami akan peroleh dengan qurban
itu?” Rasulullah menjawab: “Setiap satu helai rambutnya adalah satu
kebaikan.”Mereka menjawab: “Kalau bulu-bulunya?”Rasulullah menjawab: “Setiap
satu helai bulunya juga satu kebaikan.” [HR. Ahmad dan ibn Majah]
2. Berkurban
adalah ciri keislaman seseorang
Dari Abu
Hurairah, Rasulullah SAW bersabda: “Siapa yang mendapati dirinya dalam keadaan
lapang, lalu ia tidak berqurban, maka janganlah ia mendekati tempat shalat Ied
kami.” [HR. Ahmad dan Ibnu Majah]
3. Ibadah
kurban adalah salah satu ibadah yang paling disukai oleh Allah
Dari Aisyah,
Rasulullah SAW bersabda: “Tidak ada amalan anak cucu Adam pada hari raya qurban
yang lebih disukai Allah melebihi dari mengucurkan darah (menyembelih hewan
qurban), sesungguhnya pada hari kiamat nanti hewan-hewan tersebut akan datang
lengkap dengan tanduk-tanduknya, kuku-kukunya, dan bulu- bulunya. Sesungguhnya
darahnya akan sampai kepada Allah –sebagai qurban– di manapun hewan itu
disembelih sebelum darahnya sampai ke tanah, maka ikhlaskanlah menyembelihnya.”
[HR. Ibn Majah dan Tirmidzi. Tirmidzi menyatakan: Hadits ini adalah hasan
gharib]
4. Berkurban
membawa misi kepedulian pada sesama, menggembirakan kaum dhuafa
“Hari Raya
Qurban adalah hari untuk makan, minum dan dzikir kepada Allah” [HR. Muslim]
5. Berkurban
adalah ibadah yang paling utama
“Maka
dirikanlah shalat karena Tuhanmu; dan berkurbanlah.” [Qur’an Surat Al Kautsar :
2]
Syaikhul
Islam Ibnu Taimiyyah ra sebagaimana dalam Majmu’ Fatawa (16/531-532) ketika
menafsirkan ayat kedua surat Al-Kautsar menguraikan : “Allah Subhanahu wa
Ta’ala memerintahkan beliau untuk mengumpulkan dua ibadah yang agung ini yaitu
shalat dan menyembelih qurban yang menunjukkan sikap taqarrub, tawadhu’, merasa
butuh kepada Allah Subhanahu wa Ta’ala, husnuzhan, keyakinan yang kuat dan
ketenangan hati kepada Allah Subhanahu wa Ta’ala, janji, perintah, serta
keutamaan-Nya.”
“Katakanlah:
sesungguhnya shalatku, sembelihanku (kurban), hidupku dan matiku hanyalah untuk
Allah, Tuhan semesta alam.” [Qur’an Surat Al An’am : 162]
Beliau juga
menegaskan: “Ibadah harta benda yang paling mulia adalah menyembelih qurban,
sedangkan ibadah badan yang paling utama adalah shalat…”
6. Berkurban
adalah sebagian dari syiar agama Islam
“Dan bagi
tiap-tiap umat telah Kami syariatkan penyembelihan (kurban), supaya mereka
menyebut nama Allah terhadap binatang ternak yang telah direzekikan Allah
kepada mereka, maka Tuhanmu ialah Tuhan Yang Maha Esa, karena itu berserah
dirilah kamu kepada-Nya. Dan berilah kabar gembira kepada orang-orang yang
tunduk patuh (kepada Allah)” [Qur’an Surat Al Hajj : 34]
7. Mengenang
ujian kecintaan dari Allah kepada Nabi Ibrahim
“Maka
tatkala anak itu sampai (pada umur sanggup) berusaha bersama-sama Ibrahim,
Ibrahim berkata: “Hai anakku sesungguhnya aku melihat dalam mimpi bahwa aku
menyembelihmu. Maka fikirkanlah apa pendapatmu!” Ia menjawab: “Hai bapakku,
kerjakanlah apa yang diperintahkan kepadamu; insya Allah kamu akan mendapatiku
termasuk orang-orang yang sabar”. Tatkala keduanya telah berserah diri dan
Ibrahim membaringkan anaknya atas pelipis(nya), (nyatalah kesabaran keduanya).
Dan Kami panggillah dia: “Hai Ibrahim, sesungguhnya kamu telah membenarkan
mimpi itu sesungguhnya demikianlah Kami memberi balasan kepada orang-orang yang
berbuat baik. Sesungguhnya ini benar-benar suatu ujian yang nyata. Dan Kami
tebus anak itu dengan seekor sembelihan yang besar.” [Qur’an Surat Ash Shaffat
: 102 - 107]











 )
)


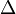 Tb = kenaikan titik didih (oC)
Tb = kenaikan titik didih (oC)




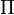 = tekanan osmotik
= tekanan osmotik
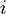 = faktor Van't Hoff
= faktor Van't Hoff = derajat ionisasi
= derajat ionisasi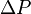 =P0
=P0

 =
=
 =
=